北理工团队筛选获得抗新冠病毒的中和核酸适配体
华体会体育(中国):2021-07-19 供稿:前沿交叉科学研究院 黄渊余
编辑:石殊伦 审核:唐水源 阅读次数:
从2019年12月开始至今,新冠病毒在全球范围内造成约一亿八千万人患病,约三百八十万人死亡。人与人之间的快速传播是SARS-CoV-2最显著的特征之一。通过Spike蛋白与宿主细胞血管紧张素转换酶(ACE2)受体结合开始侵染过程是SARS-CoV-2的主要传播机制。其中,Spike蛋白的S1亚基的RBD结构域促使SARS-CoV-2与ACE2的识别与结合;同时,S2亚基触发膜融合,介导病毒基因组注入宿主的细胞质。因此,ACE2与RBD结合的阻断被认为是抑制SARS-CoV-2侵染和传播的关键策略。目前,虽然已有瑞德西韦、氯喹、干扰素、托西珠单抗、恢复期血浆、中和抗体、中药等多种病毒和宿主疗法用于预防及治疗COVID-19,但目前尚无针对性的特效治疗药物。基于核酸的治疗剂,因其开发快、靶向特异性高以及副作用少,在新冠肺炎(或其它感染性疾病)的防治方面潜力巨大。开发一种基于核酸适配体(Aptamer)的治疗方案是控制新冠肺炎的一种潜在有效方法。
近日,华体会体育前沿交叉学科研究院黄渊余研究员团队在Signal Transduction and Targeted Therapy (中国科技期刊卓越行动计划领军期刊,IF="18.187)发表题为 Identification of SARS-CoV-2-against aptamer with high neutralization activity by blocking the RBD domain of spike protein 1 的文章,筛选和鉴定了可阻断S1亚基RBD结构域的SARS-CoV-2中和活性核酸适配体。
该研究通过基于毛细管电泳(CE)的指数富集的配体系统进化技术(CE-Based SELEX)筛选S1亚基的高亲和力、特异性的核酸适配体,为确保候选序列的亲和力和特异性的进化效率,采用了正、负和复杂背景筛选过程相结合的SELEX策略,不断降低靶蛋白的浓度以增加筛选压力,最终获得6条对S1亚基具有高亲和力的DNA适配体nCoV-S1-Apts( KD ="0.118±0.033~85.610±14.219" nM)。
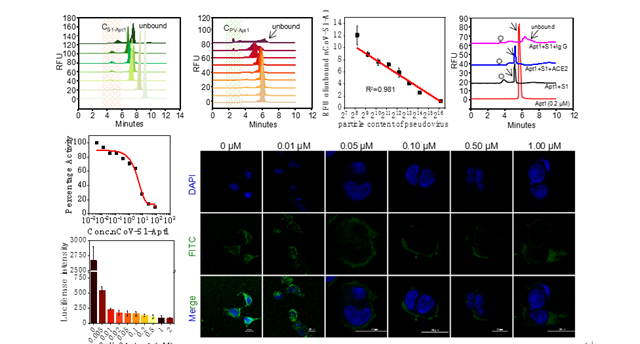
特异性与毒性评价结果表明,nCoV-S1-Apts具有高特异性、抗血浆蛋白干扰特性与低毒性,这有利于减少潜在的脱靶效应和细胞毒性。进一步,通过分子对接预测nCoV-S1-Apt1可结合于S1亚基的RBD结构域上,覆盖其与ACE2结合的两个主要活性位点,同时也通过RBD蛋白的结合实验证实了这一点,因此nCoV-S1-Apt1有潜力被用作RBD结构域的有效抑制剂。
为了评价nCoV-S1Apt1的识别和检测潜力,该研究建立了一种AuNPs比色法,可以快速、特异地检测人血清中的S1亚基,检测下限约为3.125 nM。同时,FAM标记的nCoV-S1-Apt1可被用作荧光探针捕获人血清中的S1亚基与SARS-CoV-2假病毒,在102-105个病毒颗粒范围内具有良好的识别和检测线性。
为了证实nCoV-S1-Apt1对SARS-CoV-2的多尺度抑制作用,该研究从RBD、S1亚基和假病毒3个水平进行了抑制实验。结果显示,nCoV-S1-Apt1可以通过与S1的RBD结合,阻碍S1与ACE2的识别及相互作用来降低SARS-CoV-2感染,这表明其作为一种新型抗SARS-CoV-2感染的核酸中和剂,具有良好的应用潜力。
综上所述,本研究筛选鉴定了S1蛋白的核酸适配体,验证了适配体在新冠肺炎预防、治疗和检测中的应用能力,并为设计融合型核酸抑制剂、病毒中和寡核苷酸或靶向递送系统提供了潜在工具。此外,该研究也提出了一种基于多尺度靶标的病毒中和型核酸适配体的筛选和鉴定策略。
华体会体育前沿交叉学科研究院、生命学院博士后杨歌为论文第一作者,黄渊余研究员为通讯作者。该研究得到华体会体育屈锋教授的大力支持。
论文详情:
Ge Yang, Ziyue Li, Irfan Mohammed, Liping Zhao, Wei Wei, Haihua Xiao, Weisheng Guo, Yongxiang Zhao, Feng Qu & Yuanyu Huang*. Identification of SARS-CoV-2-against aptamer with high neutralization activity by blocking the RBD domain of spike protein 1. Signal Transduction and Targeted Therapy 2021; 6(1):227. DOI: 10.1038/s41392-021-00649-6
教师主页: https://www.x-mol.com/groups/Yuanyu_Huang-BIT
论文链接: https://www.nature.com/articles/s41392-021-00649-6
分享到:
